高考无机推断题的特点及教学
长汀一中 丘凤玲
无机推断题是以前高考中每年必考的题型,也是现在理综卷和单科化学必考的题型。分别以近三年福建理综卷和江苏化学卷为例:
福建理综
|
福建理综卷 |
2003 |
2004 |
2005 | ||||
|
题 号 |
8 |
32 |
6 |
28 |
7 |
26 |
27 |
|
对应题分值 |
6 |
11 |
6 |
14 |
6 |
15 |
15 |
|
百分比 |
14.17% |
18.52% |
33.33% | ||||
江苏化学
|
江苏化学卷 |
2003 |
2004 |
2005 | ||||||||
|
题 号 |
2 |
12 |
21 |
22 |
5 |
6 |
21 |
22 |
13 |
22 |
26 |
|
对应题分值 |
4 |
4 |
6 |
12 |
4 |
4 |
12 |
6 |
4 |
10 |
10 |
|
百分比 |
17.33% |
17.33% |
16.00% | ||||||||
从上面的统计可以看出无机推断题确实是高考非常关注的题型,无论是题量还是分值都比较大。所以,在高考复习中有必要作为一个专题来复习和训练。
一、无机推断题的特点
1.无机推断题集元素化合物知识、基本概念和基本理论知识为一体。具有考查知识面广、综合性强、思考容量大的特点。这种题型不但综合性考查学生在中学阶段所学的元素及其化合物知识以及物质结构、元素周期律、电解质溶液、化学平衡、氧化还原反应、化学用语等知识,而且更重要的是它能突出考查学生的综合分析判断能力、逻辑推理能力。且结构紧凑、文字表述少,包含信息多,思维能力要求高。
2.无机推断题与双基知识、有机、实验、计算均可联系,出题比较容易。在少题量的情况下,可考多个知识点,多方面的能力,从而更好地突出学科内综合,这就受到了理综卷的青睐。
3.无机推断题层次明显,区分度高,有一步推错,整题失分的可能,很容易拉分。具有很高的区分度和很好的选拔功能。尽管它考的内容广,能力全面,层次高,但它还是离不开大纲和考纲。知识点必须是高中阶段强调掌握的基础知识和主干知识。
例题1(2005年高考理综卷)26.(15分)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
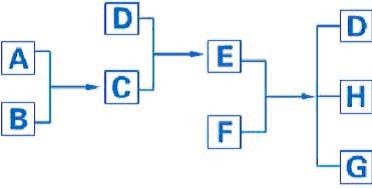
(1)D的化学式(分子式)是 ______________ ,E的化学式(分子式)是 ____________________
(2)A和B反应生成C的化学方程式是____________
(3)E和F反应生成D、H和G的化学方程式是_________________________
这道题就是以NH3 的实验室制法,NH3 、HCl的性质为知识点出的,涉及到的知识点高中阶段相当重要,但比较简单。
答案 (1)NH3 NH4Cl
(2)H2+Cl2
(3)2NH4Cl+Ca(OH)2
例题2(2004年高考理综卷Ⅱ)28.(14分)在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几
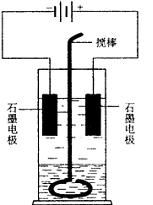 (1)阳极上的电极反应式为___________________。
(1)阳极上的电极反应式为___________________。
(2)阴极上的电极反应式为___________________。
(3)原上层液体是_______ ______。
(4)原下层液体是____________ ___。
(5)搅拌后两层液体颜色发生变化的原因是_ _。
(6)要检验上层液体中含有的金属离子,其方法是____________,现象是_____________________。
它立意的知识点也相当基础,就是将简单的电化学,基本的卤族性质,萃取,焰色反应揉合在一起了,当时可考倒了许多考生,这道题目的得分相当
答案:
因而教师和学生在复习时都必须把握好高中阶段的基础知识和主干知识。
二、 无机推断题“题眼”总结
物质推断涉及知识面广,思维强度大,问题的核心在于如何确定解题的突破口。下面将有关题眼总结如下:
1、同一元素的气态氢化物和气态氧化物反应,生成该元素的单质和水,该元素可能是硫或氮。
2、同一元素的气态氢化物和最高氧化物对应的水化物化合,生成盐的元素一定是氮。
3、两溶液混合生成沉淀和气体,这两种溶液的溶质可能分别是:①Ba(OH)2与(NH4)2SO4,②可溶性铝盐与可溶性金属硫化物或可溶性碳酸盐或碳酸氢盐,③可溶性铝铁盐与可溶性碳酸盐或碳酸氢盐。
4、既能与酸反应,又能与碱反应的物质可能是Al、Al2O3、Al(OH)3、氨基酸、弱酸的铵盐、弱酸的酸式盐等。
5、既能与强酸反应放出气体又能与强碱反应放出气体,常见的物质有Al、弱酸的铵盐(如碳酸铵、碳酸氢铵、亚硫酸铵、硫化铵、硫氢化铵等)。
6、在水中分解生成气体和难溶物或微溶物的物质可能是Al2S3、Mg3N2、CaC2等。
7、与水接触放出气体的常见物质有:Li、Na、K、Na2O2、F2。
8、 A物质放到B物质中,先生成沉淀,后沉淀又溶解,A、B可能分别是CO2与Ca(OH)2、NaOH与铝盐、NH3与AgNO3、HCl与NaAlO2。
9、使溴水褪色的物质有H2S、SO2、不饱和烃类、活泼金属、碱类等。
10、特殊的实验现象:
(1)H2在Cl2中燃烧呈苍白色火焰。
(2)钠元素的焰色反应为黄色,钾元素的焰色反应为浅紫色。
(3)遇酚酞变红的气体必是氨气。
(4)在空气中迅速由无色变为红棕色的气体是NO。
(5)Cl2通入含Br-溶液中,会出现橙色;加入有机溶剂,在有机溶剂层出现橙红色。Cl2通入含I-的溶液中,会出现深黄色,加入有机溶剂,在有机溶剂层出现紫红色。
(6)遇SCN-显红色或OH-遇生成红褐色沉淀或遇苯酚显紫色的离子是Fe3+。
(7)遇BaCl2溶液生成白色沉淀的溶液中可能含有Ag+或SO42-。
(8)遇HCl生成沉淀的溶液中可能含有Ag+、SiO32-、S2O32-。
(9)具有臭鸡蛋气味的气体是H2S,与H2S反应生成淡黄色沉淀的气体可能是Cl2、O2、SO2、NO2等。
(10)电解电解质溶液时阳极气态产物一般是Cl2或O2,阴极气态产物是H2。
(11)使品红褪色的气体可能是或,物质可能是次氯酸盐,如、,氯水、等。
(12)溶液中一些离子的颜色,Cu2+:绿色(浓的CuCl2溶液中)或蓝色(其它的铜盐溶液或CuCl2的稀溶液中)。Fe3+:棕黄色(浓溶液)或黄色(稀溶液)。Fe2+:浅绿色。MnO4-:紫红色。
(13)某些沉淀的颜色:
Fe(OH)3:红褐色。Fe(OH)2:白色沉淀,迅速地转变成灰绿色,最后变成红棕色沉淀。
CuS、Ag2S、PbS黑色沉淀均不溶于酸。FeS:黑色沉淀溶于酸。
AgBr:淡黄色沉淀,不溶于酸。
AgI、Ag3PO4:黄色沉淀,其中Ag3PO4溶于酸,而AgI不溶于酸。
在含有S2-的酸性溶液中,加入能与它反应的氧化剂(Cl2、O2、SO32-、NO3-、Fe3+ 等)会出现黄色沉淀。
11、常见无机反应的组合类型(反应物、产物种数组合关系):
(1)1→3:2KMnO4 == K2MnO4 + MnO2 + O2↑
Cu2(OH)2CO3 == 2CuO + H2O + CO2↑
NH4HCO3 == NH3↑ + H2O + CO2↑
(2) 2→3:
X2、S与碱液的反应:
例 Cl2 + 2NaOH == NaCl + NaClO + H2O
3S + 6KOH(热) == 2K2S + K2SO3 + 3H2O
Cu、Zn、Fe、Al与氧化性酸的反应:
例 3Cu + 8HNO3(稀) == 3Cu(NO3)2 + 2NO↑ + 4H2O
电解NaCl(KBr、Na2S等)、CuSO4、AgNO3水溶液:
例:2NaCl + 2H2O ==== 2NaOH + H2↑ + Cl2↑(条件:电解)
(3)2→4:Na2S2O3 + H2SO4 == Na2SO4 + S↓ + SO2↑ + H2O
2KmnO4 + 16HCl == 2MnCl2 + 2KCl + 5Cl2↑ + 8H2O
(4)3→3:2Na2S + Na2SO3 + 3H2SO4 == 3Na2SO4 + 3S↓ + 3H2O
KIO3 + 5KI + 3H2SO4 == I2 + 3K2SO4 + 3H2O
KclO3 + 5KCl + 3H2SO4 == 3K2SO4 + Cl2↑ + 3H2O
(5)3→4:2NaCl + MnO2 + 2H2SO4 == Na2SO4 + MnSO4 + Cl2↑ + 2H2O
Na2S + Na2SO3 + H2SO4 == Na2SO4 + S↓ + SO2↑(H2S) + H2O
三、无机推断题的教学体验
无机推断题考查知识面广,考题内容多为常见元素及其化合物知识,常与双基知识、有机、实验、计算联系,试题的容量比较大。但推断的物质不会超出中学范围所学的元素及其化合物知识,要学生书写的内容也不过是常用的化学用语。这类试题学生失分的原因有以下几点:一是学生对元素及其化合物的知识不够全面与熟悉;二是学生的分析判断能力与逻辑推理能力欠缺;三是学生的化学用语掌握不够;四是学生对这种试题练习不够,有一种恐惧心理;五是学生缺乏对这种题型的解题思路。因此,要想帮助学生解好推断题,教师要指导学生对这种试题做专题训练,在专题训练的时候,一要做学生的思想工作,让他们了解无机推断题的特点与考查的知识点与能力要求;二要求学生自己整理或帮助学生整理归纳元素及其化合物知识,要让他们熟练掌握一些特征的性质与变化;三要通过示例分析总结出常见的解题思路与方法;五要让学生训练考查不同知识点与不同解题思路的的各种试题,让他们在训练中找感觉,同时教师要认真批改学生的练习,并及时纠正他们的化学用语的表达,以求达到科学化、标准化。
另外,注意学生答这类题时常见的错误:如把答案写在密封线内,阅卷时无法看到答案而不给分;要求写元素名称而错写成元素符号,而要求写元素符号又答成元素名称或分子式;要求写物质名称而错写成分子式;要求写结构简式的错写成分子式或名称;要求写离子方程式而错写成化学方程式;要求画离子结构示意图而错答为原子结构示意图;把相对原子质量、相对分子质量、摩尔质量的单位写成“克”;把物质的量、摩尔浓度、气体体积、质量、溶解度、密度、压强等的单位漏掉;化学方程式、离子方程式不配平;热化学方程式不注明物质的状态等;还有的没把整题看懂,能答得出的有些问都不答。因此答题时必须按题目要求来回答,规范学生的答题行为,同时要鼓励学生敢于答这种题。
 扫一扫关注我们
扫一扫关注我们